Reatividade e orientação na substituição eletrófila
Por Redação
16 – Reatividade e orientação na substituição eletrófila
A) Grupos desativantes
Todos os grupos que estiverem ligados ao núcleo benzênico serão considerados elétrons atraentes e irão orientar a introdução de outro grupo para a posição meta. Estes grupos irão desativar o núcleo benzênico e com isso diminuir a velocidade da reação, como exemplo, podemos citar o nitrobenzeno, que é quase um milhão de vezes menos reativo do que o benzeno.
Esse núcleo benzênico irá ser atacado pelo cátion B+, ou seja, um grupo elétron atraente que pode puxar elétrons deste núcleo, fazendo com que ele fique menos suscetível ao ataque do cátion B+ e mais positivo.
Os metas são orientados pelos grupos insaturados ou por grupos que possuem ligação dativa.
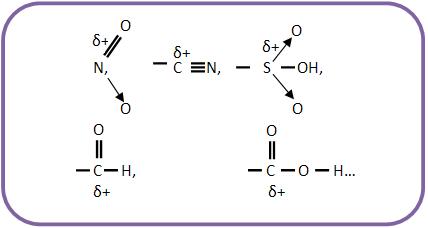
O átomo que está ligado ao núcleo benzênico, fica polarizado positivamente. Esse grupo pode puxar elétrons do núcleo benzênico.
Mesmo que o grupo abaixo seja saturado, ele é desativante, pois o carbono pode estar polarizado positivamente.
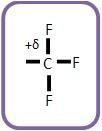
B) Grupos ativantes
Todos os grupos que estiverem ligados ao núcleo benzênico serão considerados elétrons repelentes e irão orientar a entrada de outro grupo para as posições orto ou paradirigentes. Estes grupos irão ativar o núcleo benzênico e com isso aumentar a velocidade da reação, como exemplo, podemos citar a anilina, que é quase um milhão de vezes mais ativa que o benzeno.
Esse grupo de elétrons que repelem, tem a intenção de empurrar os elétrons direto para o núcleo benzênico, fazendo com que ele fique mais suscetível ao ataque do cátion B+, e mais negativo.
Esses grupos saturados orientam as posições para os paradirigentes e orto.
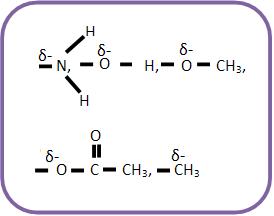
O átomo ligado ao núcleo benzênico fica polarizado negativamente. Esse grupo pode empurrar elétrons para o núcleo benzênico.

 Conceito de Sulfonação
Conceito de Sulfonação