Energia interna
Por Redação
energia interna (U)
É a soma de todas as modalidades de energia que um sistema possui em seu interior.
U = EQ + ET
É considerada energia interna, quando um sistema é capaz de realizar um trabalho.
Existem alguns tipos de energia interna, como: a energia cinética de translação das partículas, a energia cinética de rotação das partículas e a energia potencial de ligação entre as partículas.
Quando falamos de energia interna em relação aos gases perfeitos, podemos considerar a energia cinética de translação das moléculas, sendo representada pela seguinte expressão:
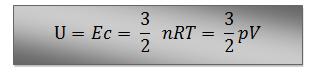
A partir das afirmações acima, podemos concluir que, a energia interna de certo número de mols de um gás perfeito, é totalmente dependente da temperatura, e que a energia interna de um determinado número de mols de um gás perfeito, é diretamente proporcional à temperatura absoluta do gás.
Para calcularmos a relação entre a temperatura de um gás perfeito e a velocidade média de suas partículas, temos que usar a seguinte função:
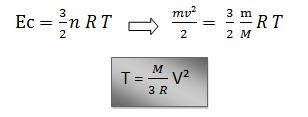
Com base nas funções acima, podemos afirmar que a temperatura de um gás perfeito, sempre será proporcional ao quadrado da velocidade média das moléculas.
Podemos observar que para um determinado gás, a temperatura é totalmente dependente da velocidade das moléculas e que as moléculas são totalmente dependentes da temperatura.
Portanto, a relação entre a temperatura e velocidade, demonstra que quando um varia o outro também varia, quando um é constante o outro também será constante.
Desse modo, a temperatura de um determinado número de moléculas de um gás perfeito é trabalho restrito à energia cinética de suas moléculas.
Assim, podemos dizer que a energia interna de um sistema varia diretamente com a temperatura.

*Exceto nas mudanças de estado.
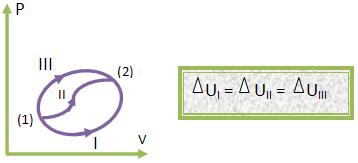
A variação de energia interna é independente dos estados intermediários.
Importante: Em um ciclo, a variação de energia interna sempre será nula, ou seja, delta U = 0. Veja a representação no diagrama: