Mecanismo da adição em alcenos
Por Redação
7 – Mecanismo da adição em alcenos
Com a insaturação nos alcenos é possível a união da molécula a outros átomos (reação de adição), deixando a molécula de um alqueno bem mais reativa que a de um alcano, como exemplo: o gás etileno que acrescenta cloro (à temperatura ambiente, sem necessidade de luz) resultando no líquido dicloroetano. Por se transformarem em hidrocarbonetos gasosos em di-haletos líquidos, os alquenos foram denominados olefinas, que são formadoras de óleos.
A adição eletrofílica é um tipo de adição feita nos alquenos, fazendo com que os hidrocarbonetos etilênicos funcionem como base de Lewis. Já todos os receptores de elétrons são denominados agentes eletrofílico, portando-se como ácido de Lewis.
Os grupos que fornecem agente eletrofílico são:
Cl2, Br2, I2, HI, HBr, HCl , H2SO4, HOCl
Considerando o grupo AB, podemos observar que a molécula AB se decompõe, formando o seguinte par d íons:
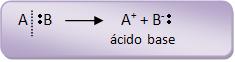
Na primeira fase ocorre o ataque dos átomos de carbono insaturado pelo íon positivo A+. Cria-se uma espécie intermediária (íon carbônio) junto com uma carga positiva no outro átomo de carbono.
Vejamos:
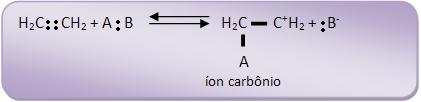
Na segunda fase, o íon carbônio combina-se com o íon B–.
Vejamos:
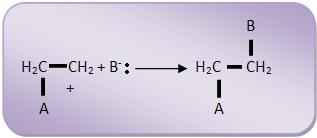
A velocidade é controlada pela primeira fase.
A) Cloração do eteno
1° fase

2° fase
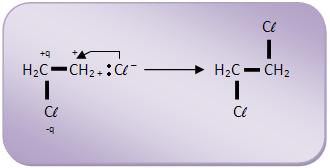
A adição é trans, onde os átomos de cloro chegam mais perto da molécula por lados opostos e o átomo de cloro do íon carbônio é considerado um pólo negativo que repele o íon Cl -, que ataca o íon carbônio pelo outro lado. Não pode ser comprovado tal experimento, pelo fato da possibilidade de uma livre rotação em volta da ligação simples, já na adição em compostos cíclicos a rotação irá se restringir através do ciclo, onde o produto inicial da adição é o trans.
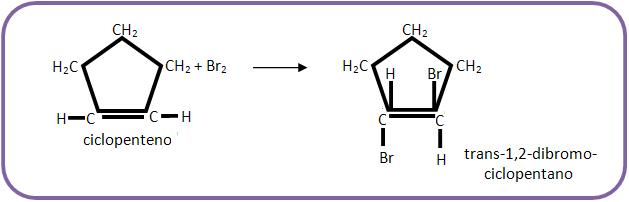
B) Adição de haletos de hidrogênio (HX)
B.1) Regra de Markovnikov
“Nas reações de adição, o elemento eletropositivo (geralmente o hidrogênio) tem a propriedade de fixar-se no carbono mais hidrogenado”.
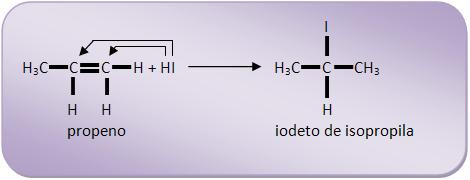
B.2) Mecanismo da Reação de Markovnikov
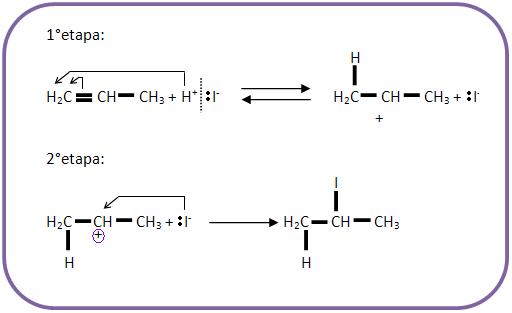
Portanto podemos concluir que quanto mais ácida a substância que atacar o alceno, maior será a reatividade. Com isso a ordem decrescente facilitará a adição.
Vejamos:
HI > HBr > HCl
