Compostos de Cadeia Cíclica
Por Redação
Acontece, porém, que a dupla ligação (o par ligação s + p) não pode “girar”, como ocorre com a ligação simples; isto significa, em outras palavras, que as duas figuras anteriores são “rígidas”. Sendo assim, não há maneira de superpor a forma cis sobre a forma trans, de modo a coincidirem todos os seus átomos. Conseqüentemente, as formas cis e trans representam dois compostos diferentes. Podemos representá-los abreviadamente do seguinte modo:
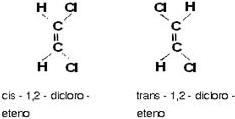
Generalizando, podemos dizer que irá ocorrer isomeria cis-trans em compostos contendo dupla ligação e que apresentem a estrutura:
![]()
Sendo obrigatoriamente R1 R2 e R3 R4 e podendo R1 (ou R2) ser igual ou diferente de R3 e R4.
Em Compostos de Cadeia Cíclica
Quando estudamos compostos cíclicos, podemos observar o seguinte comportamento:
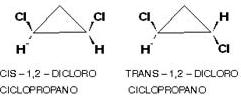
Resumindo, o composto 1,2 dicloro ciclopropano pode apresentar as suas ramificações “acima” ou “abaixo” do plano que forma o núcleo do composto sendo classificado como cis ou trans.
