Mudança de estado de substância pura e mistura
Por Redação
8. Mudança de estado de substância pura e mistura
Introdução
Para diferenciarmos a mistura da substância pura, é só observarmos o comportamento de cada uma na hora do aquecimento, sob a pressão constante, pois é a partir do aquecimento de um líquido que podemos ver se é ou não uma substância pura.
Substância pura
A temperatura de uma substância se mantém constante quando o seu estado físico é alterado. Quando gelo é aquecido a temperatura varia a medida que o tempo passa.
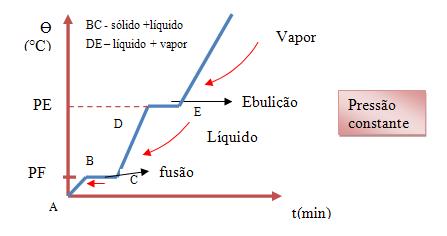
Onde PF é = ponto de fusão e PE é = ponto de ebulição.
Mistura comum
A temperatura de uma mistura não permanece constante durante todo o processo da mudança de estado. Vejamos agora dois gráficos, um que nos mostra a solidificação de água salgada, e outro que nos mostra o aquecimento de água doce:
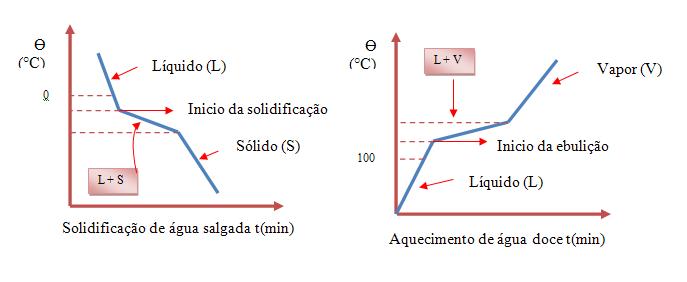
Com isso podemos concluir que uma mistura comum, pode apresentar tanto ponto de fusão, como ponto de ebulição, ambos podendo ser variáveis.
Mistura especiais
Podem ser chamadas de misturas eutéticas ou eutético e azeotrópicas ou azeotrópicos, são misturas que durante a fusão, solidificação, ebulição e condensação, se portam como substâncias puras.
– Misturas eutéticas
Com relação à fusão e à solidificação, as misturas eutéticas, se portam exatamente como fossem as substâncias puras, ou seja, elas têm o seu ponto de fusão constante.
Observando o topo das fusões, notamos que a temperatura da fusão de um eutético é inferior com relação à dos seus componentes.
Observe o exemplo:
Cádmio (40%) e bismuto (60%)
Cádmio puro PF = 320ºC
Bismuto puro PF = 280ºC
Eutético PF = 140ºC
(P.F, ponte de fusão)
Vejamos o gráfico abaixo:
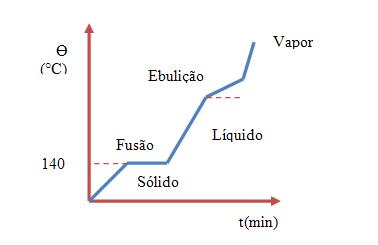
– Misturas azeotrópicas
Essas misturas se portam como substâncias puras, no processo de ebulição, portanto seu ponto de ebulição é constante. Quando se tem uma mistura de 4% de água com 96% de álcool é considerada uma mistura azeotrópica, permanecendo constante durante todo o processo de ebulição, sem que o sistema se desfaça em seus componentes.
Observe o exemplo:
Álcool (96%) e água (4%)
Água pura PE = 100ºC
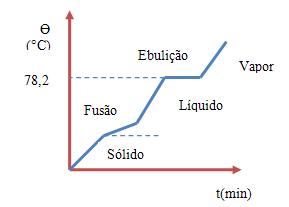
Álcool puro PE = 78,3ºC
Mistura azeotrópica PE = 78,2ºC
(P.E, ponte de ebulição)
Vejamos a ilustração abaixo:
Se quisermos representar essa mistura graficamente, ficara assim: