Cálculo de equivalente
Por Redação
3. Cálculo de equivalente
• elemento químico
![]()
Exemplos:

• Ácido
![]()
Exemplos:
Na reação:
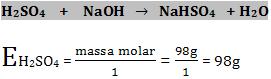
O equivalente-grama de um ácido é definido como a massa que possui ou pode fornecer 1 mol de H+ (6,02 x 1023 íons de H+).
Se ocorre a dissociação do ácido sulfúrico da seguinte forma:
![]()
Logo temos:
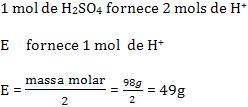
• base
![]()
Exemplo:
Na reação:

O equivalente-grama de uma base é definido como a massa que possui ou pode fornecer 1 mol de OH– (6,02 x 1023 íons OH–).
Se ocorrer a dissociação do hidróxido de magnésio da seguinte forma:
![]()
Logo temos:

É importante lembrar que: 1 equivalente-grama de ácido reage exatamente com 1 equivalente-grama de base.
• Sal
![]()
Exemplo:
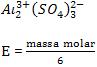
• Oxidantes e redutores

Exemplo:
Na reação não balanceada:
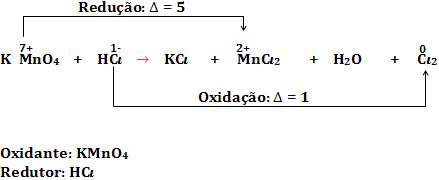
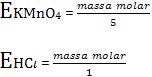
Equivalente-grama de um redutor é definida como a massa que fornece 1 mol de elétrons (6,02 x 1023 elétrons).
Equivalente-grama de um oxidante é definida como a massa que recebe um mol de elétrons (6,02 x 1023 elétrons).
Lembre-se: 1 equivalente de redutor reage exatamente com 1 equivalente de oxidante.
