Os Eletrólitos
Por Redação
4. Os eletrólitos
Os eletrólitos são compostos que quando são colocados em contato com a água, originam soluções eletrolíticas, podendo ser tanto de natureza covalente, como de natureza iônica.
Eletrólitos de natureza iônica
Sabe-se que em condições ambientais os compostos iônicos estão no estado sólido, nos eletrólitos eles constituem uma espécie de retículo, ficando retidos nesses retículos, nesse estado não é possível que conduzam corrente elétricas.
Ao ser colocado o eletrólito em contato com a água, esse retículo irá se quebrar.
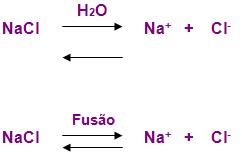
Dissociação iônica: é o processo de separação dos íons.
Eletrólitos covalentes (moleculares)
É a reação entre os compostos covalentes quando colocados na água provocam o surgimento de íons que fazem com que a solução seja condutora de corrente elétrica.
Por exemplo:
Coloca-se HCl na água, acontecerá uma reação. Vejamos a ilustração abaixo:
H3O+ (hidroxonio ou hidrônio) é a ligação entre o íon H e a molécula de H2O, observe abaixo a reação de forma simplificada:
![]()
Os íons surgiram a partir da reação, pois no composto HCL, não estavam presentes esses íons.
Ionização: é o processo que por uma reação forma íons no composto.
Para exemplificar a diferença:
Dissociação separa os íons do retículo cristalino. Vejamos:
![]()
Ionização forma os íons pela reação existente entre a molécula do eletrólito e a molécula da água.
![]()
