Calor trocado nos processos sob pressão constante – entalpia
Por Redação
8. Calor trocado nos processos sob pressão constante – entalpia
A maioria das reações químicas ocorre em recipientes abertos. No decorrer desses processos pode ocorrer a variação no volume do sistema, já a pressão feita pela atmosfera é sempre constante. Quando a expansão dos gases em recipiente aberto empurra a atmosfera, realiza-se trabalho P∆V.
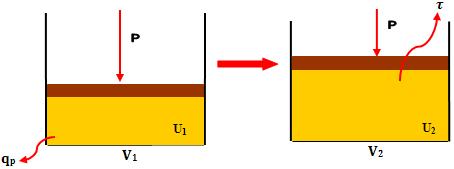
Onde, qp é o calor trocado a pressão constante, logo temos:
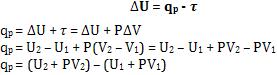
Desse modo, podemos notar que o calor trocado a pressão constante é dado pela diferença entre dois termos, cada um deles tem a forma:
U + PV
Tal função é chamada entalpia do sistema, simbolizada por: H
H = U + PV
Logo, o calor trocado a pressão constante é dado por:
qp = H2 – H1 = ∆H
onde, ∆H é a variação de entalpia que ocorre na reação química.
