Deslocamento do Equilíbrio Químico
Por Redação
Deslocar um equilíbrio químico significa fazer que a velocidade da reação direta fique diferente da velocidade da reação inversa (v1 v2).
Importância
O deslocamento da equilíbrio químico é um artifício largamente utilizado nos processos industriais para melhorar a obtenção de determinadas substâncias.
Exemplo: Síntese de Haber–Bosch – É a produção da amônia à altíssima temperatura de 500°C, altíssima pressão de 200atm e na presença de ferro como catalisador.
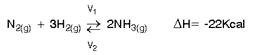
Princípio regedor do deslocamento do equilíbrio químico: Princípio de Le Chatelier (Fugante a força)
“Quando um sistema em equilíbrio sofre a ação de forças externas, o sistema tende a se deslocar no sentido de minimizar a ação da força aplicada, procurando uma nova situação de equilíbrio.”
Fatores capazes de deslocar o equilíbrio:
1. Concentração (Guldberg–Wage)
2. Temperatura (Van’t Hoff)
3. Pressão (Robin)
Observação – O catalisador não desloca um equilíbrio químico, pois aumenta igual e simultaneamente ambas as velocidades v1 e v2, porém faz que o equilíbrio seja atingido mais rapidamente.
1. Influência da concentração no equilíbrio químico:
O aumento da concentração de uma substância presente no equilíbrio faz que o equilíbrio se desloque no sentido de consumir a substância adicionada, isto é, o equilíbrio se desloca para o lado contrário ao aumento. Já a diminuição de uma substância presente no equilíbrio faz que o equilíbrio se desloque no sentido de repor a substância retirada, isto é, o equilíbrio se desloca para o mesmo lado da diminuição.
Observações:
1. Substância sólida não desloca um equilíbrio químico, pois a concentração de um sólido em termos de velocidade é considerada constante, porque a reação se dá na superfície do sólido.
2. Substância líquida em excesso não desloca o equilíbrio químico quando alterada a sua concentração, pois a concentração de um líquido em excesso em termos de velocidade é considerada constante, porque o líquido em excesso não é fator limitante da reação.
3. Pulverizando uma substância sólida, o equilíbrio desloca-se para o lado contrário a pulverização, pois aumenta a superfície de contato, aumenta o número de colisões efetivas e, conseqüentemente, aumenta a velocidade da reação.
4. Alterando-se a concentração de uma substância presente no equilíbrio, o equilíbrio desloca-se, porém sua constante de equilíbrio permanece inalterada (a constante permanece constante).
